メチル化によるヒストンタンパク質構造変化の初観測
―DNA損傷修復機構の解明とエピジェネティック創薬の進展に期待―
発表のポイント
- ●DNA損傷修復を始め、様々な細胞内の機能に関わるヒストンタンパク質H3の溶液中の構造が、たった一つのアミノ酸残基のメチル化により大きく変化することを発見
- ●放射線などの環境ストレスによって生じるDNA損傷の修復機構の全容解明に寄与
- ●ヒストンの修飾制御により薬効を得るエピジェネティック薬の開発進展に大きく貢献すると期待
概要
国立大学法人広島大学放射光科学研究センター(以下、「HiSOR」という)の泉雄大助教、松尾光一准教授、生天目博文教授、谷口雅樹名誉教授と国立研究開発法人量子科学技術研究開発機構量子ビーム科学研究部門の藤井健太郎上席研究員、横谷明徳上席研究員らの研究チームは、HiSORの放射光*1円二色性*2分光装置を用いて、DNA二重鎖切断損傷*3修復機構に関わる9番目のリジン残基*4がトリメチル化*5したヒストンタンパク質*6H3(以下、単に「トリメチル化H3」という)の溶液中の構造*7を調査し、その構造がメチル化していない通常のH3とは大きく異なることを発見しました。この構造変化は、DNA損傷修復の過程において不可欠な現象であると予想されます。
泉助教らはこれまでに、放射線で傷ついたDNAを修復している途中の細胞の中では、DNAと共に染色体*8を構成しているヒストンと呼ばれるタンパク質の構造が変化することを明らかにしましたが、このような構造変化を誘発する要因は未解明でした。泉助教らは、DNA二重鎖切断損傷の修復過程でヒストンが様々な翻訳後修飾*9を受けることに着目し、DNA修復中の翻訳後修飾がヒストン構造変化の原因ではないかと考えました。そこで今回、トリメチル化H3の溶液中の構造を調べたところ、メチル化していない通常の場合と比べて、らせん状の構造が減少し、直鎖状の構造が増加することがわかりました(下図)。また、トリメチル化の前段階であるモノメチル化、あるいはジメチル化したH3の場合、トリメチル化H3とは逆に、らせん状の構造が増加し、直鎖状の構造が減少することがわかりました。
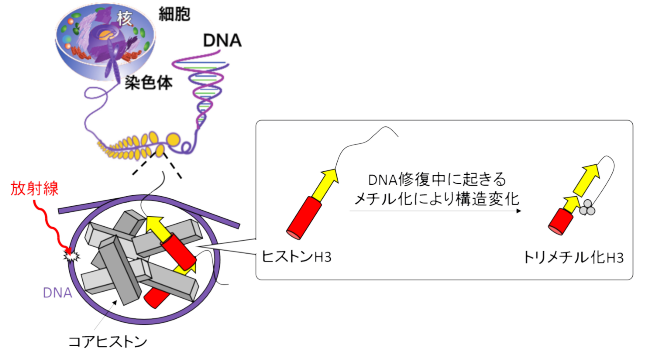
図.
DNAはコアヒストン(ヒストンタンパク質の複合体)に巻き付いて細胞核の中に収納されています。放射線などによりDNA損傷が生じると、その修復過程でヒストンが翻訳後修飾されます。今回、翻訳後修飾の一種であるトリメチル化により、ヒストンH3のらせん状の構造(赤円柱)が減少し、直鎖状構造(黄色矢印)が増加することが明らかになりました。
これまで、メチル化H3がDNA二重鎖切断損傷の修復過程で、修復に関わるタンパク質と結合するなど、重要な役割を果たしていることは知られていましたが、メチル化によりその構造が変化すること、また、付加されるメチル基の数で変化の仕方が異なることを、今回初めて明らかにしました。
今後、リン酸化、アセチル化など他の翻訳後修飾に伴う構造変化の有無や、構造変化したヒストンと他の分子との相互作用などを詳しく調べることで、傷ついたDNAを細胞が自ら修復するメカニズムの全容が解明できるようになると期待されます。このような研究を進めていくことで、将来、ヒストンの修飾を人工的に制御することで抗がん作用などの薬効を得る「エピジェネティック薬」*10の開発にもつながると期待されます。
本研究の成果は、日本放射線影響学会の英文機関紙「Journal of Radiation Research」誌に、ロンドン時間の2017年12月13日(水)午前8時(日本時間:2017年12月13日午後5時)に掲載されました。
- 雑誌名:Journal of Radiation Research
- 論文題目: Circular dichroism spectroscopic study on structural alterations of histones induced by post-translational modifications in DNA damage responses: Lysine-9 methylation of H3
- 著者:Yudai Izumi, Koichi Matsuo, Kentaro Fujii, Akinari Yokoya, Masaki Taniguchi, and Hirofumi Namatame
- doi:10.1093/jrr/rrx068
広島大学お知らせ
【研究成果】メチル化によるヒストンタンパク質構造変化の初観測 -DNA損傷修復機構の解明とエピジェネティック創薬の進展に期待-
本研究は、HiSORの共同研究委員会により採択された研究課題(課題番号:16AU007)のもと実験が行われました。また、本研究は、日本学術振興会科学研究費補助金 若手研究(B)(課題番号:JP15K16130、JP17K12825)による助成を受けて実施されました。
背景
DNAには遺伝情報が書き込まれているため、紫外線や活性酸素、放射線などの刺激によりDNAが傷つくと、正しい情報を伝えることができなくなります。その結果、正常な機能が失われたり、がんを発症したりといった重篤な影響を及ぼすことが知られています。私たちが受けるDNA損傷の数は、1日1細胞あたり5万とも50万とも言われますが、その影響をほとんど意識することなく私たちが日常生活を送れているのは、細胞が傷ついたDNAを直ちに修復しているからです。
DNA損傷を修復するメカニズムの研究は、古くから盛んに行われてきました。近年、DNAと共に染色体を構成しているヒストンと呼ばれるタンパク質が、傷ついたDNAの修復に重要な役割を果たしていることが徐々に明らかになってきました。私たちの研究グループは、これまでにDNAの修復中に細胞の中でヒストンの構造が変化することを発見していましたが、その構造変化の原因は明らかになっていませんでした。私たちはDNAの損傷を修復する途中でヒストンが受ける翻訳後修飾が構造変化を引き起こす原因ではないかと考え、これを調査しました。タンパク質の構造を調べる場合、タンパク質の結晶とX線を使う方法(X線結晶構造解析)が一般的です。しかし、この方法ではタンパク質結晶を作成する必要があり、さらに今回のような翻訳後修飾という微細な化学変化に伴う構造変化が結晶中と細胞中とで同一であることの実証も必要となります。今回私たちは、結晶作製を必要とせず、さらに生体内の環境に近い水溶液の状態でタンパク質の部分的な構造がわかる円二色性分光測定という手法を初めて用いることで、翻訳後修飾に伴うヒストンの構造の変化を観測することを試みました。
研究成果の内容
私たちの研究グループは、DNA損傷修復に関わる「9番目のリジン残基がメチル化したH3」の溶液中の構造を、HiSOR(図1)の放射光円二色性装置(図2)を用いて、近紫外から真空紫外領域までの円二色性を高精度で測定し、その構造を詳しく調査しました。比較のために、メチル化していない通常のH3の構造も同様の方法で調査しました。

図1. 広島大学放射光科学研究センター(HiSOR)の実験ホール

図2. 放射光円二色性装置 放射光は光弾性素子で円偏光に変調され、ヒストン溶液が設置された試料槽を通過する。ヒストンの円二色性シグナルは、透過光検出器で検出されます。
図3に示した円二色性スペクトルを比較すると、通常のH3とメチル化したH3ではスペクトルの形が異なることがわかります。円二色性スペクトルの形は、タンパク質の立体構造を強く反映しているので、この結果は、メチル化によってヒストンの立体構造が変わったことを意味しています。さらに、メチル基が1個ついたモノメチル化H3と2個ついたジメチル化H3の構造(スペクトル)にほとんど差がないのに対して、メチル基が3個ついたトリメチル化H3の構造(スペクトル)は、全く異なることがわかりました。詳細にスペクトルを解析すると、モノメチル化、ジメチル化H3の場合には、メチル化されていない場合に比べて、α-ヘリックスと呼ばれるらせん状の構造の割合が増加し、β-ストランドと呼ばれる直鎖状の構造の割合が減少していることが明らかになりました。一方で、トリメチル化H3の場合には、逆にα-ヘリックスの割合が減少し、β-ストランドの割合が増加しました(図4)。
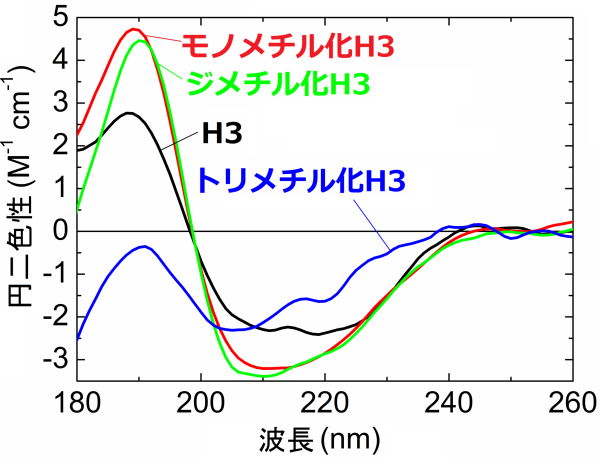
図3. モノメチル化(赤)、ジメチル化(緑)、トリメチル化H3(青)とメチル化していない通常のH3(黒)の円二色性スペクトル。
スペクトルの形はタンパク質の構造を反映するので、スペクトルを見比べてその形が違えば、タンパク質の構造が異なっていることがわかります。
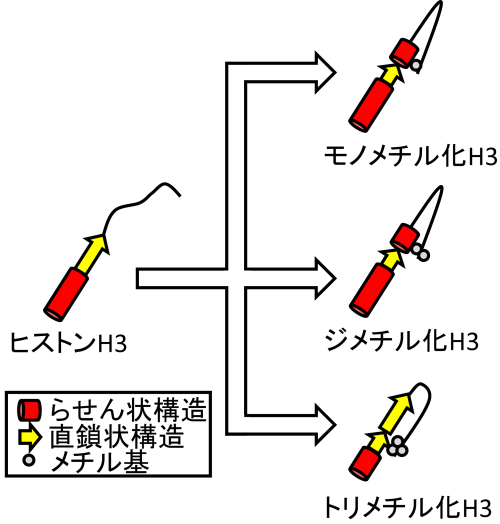
図4. メチル化による構造変化のイメージ図
(左)通常のヒストンH3は、らせん状の構造(赤円柱)、直鎖状の構造(黄色矢印)、決まった構造を持たない部分(曲線)をもちます。
(右上)H3にメチル基(灰丸)が1個つくと、その影響で直鎖状構造がらせん状構造に変化します。
(右中央)H3にメチル基が2個ついた場合も1個の場合と同様に変化します。
(右下)H3にメチル基が3個つくと、らせん状構造が直鎖状構造に変化します。
さらに、VUVCD-NN法*11と呼ばれる方法を用いて、円二色性スペクトルの解析結果とH3のアミノ酸配列から、α-ヘリックスおよびβ-ストランドを形成する位置を予測しました。その結果、メチル基がついた部分の近くだけではなく、遥かに離れた位置でも構造変化が起きていることが予測され、メチル化がH3の構造に及ぼす影響は、H3分子全体に広がっていることがわかりました。
本研究では、H3だけが存在する環境下での構造を調査しましたが、実際の細胞の中では、H3は他のヒストンタンパク質やDNAと複合体を形成しています。複合体の状態でH3の9番目のリジン残基がメチル化されたとき、その構造変化が他のヒストンタンパク質の構造にも影響を与える可能性も考えられます。タンパク質同士の相互作用の大きさは、それぞれのタンパク質の構造によって左右されます。したがって、ヒストンタンパク質とDNA修復に関わるタンパク質との相互作用は、翻訳後修飾が引き起こすヒストンタンパク質の構造変化によって制御されている可能性が考えられます。
今後の展開
本研究により、135のアミノ酸がつながってできたヒストンH3の内、たった一つのアミノ酸がメチル化されるとH3全体の構造に変化が生じること、また、付加するメチル基の数により構造変化の仕方が大きく異なることが初めて明らかになりました。ヒストンタンパク質は、DNAの修復過程で、H3のメチル化以外にも様々な種類の修飾を受けることが知られています。これらの修飾も同様に、大きな構造変化を引き起こす可能性が考えられます。今後、他の修飾に伴うH3、あるいは他のヒストンタンパク質の構造変化や、構造変化したヒストンと他の分子との相互作用などをより詳細に調査することで、傷ついたDNAを細胞が自ら修復するメカニズムの全容が解明できるようになると期待されます。
また、今回調査したH3の9番目のリジンのメチル化は、DNAの転写活性化、抑制化*12の制御といった他の細胞機能にも重要な役割を果たしていると考えられています。現在、薬剤を用いてヒストンの修飾を人工的に制御することで、がん細胞のDNAの転写を抑制し、がん細胞の増殖を防ぐ新たな抗がん剤の開発が試みられています。本研究の成果は、こういった「エピジェネティック薬」の開発の進展にも寄与すると期待されます。
用語説明
- *1 放射光
- 光速で直進する電子の進行方向が磁石などによって変えられた際に発生する電磁波。真空紫外領域からX線にわたる強力な光源であり、固体物理や生体物質構造研究をはじめ、物理・生物・化学・電子工業分野で広く利用されています。 戻る
- *2 円二色性
- 電場ベクトルがらせんを描きながら進む光を円偏光と言い、らせんの回転方向により左円偏光と右円偏光に分けられます。円偏光が物質を通過するとき、左右の円偏光の吸収の度合いに差が生じる現象を円二色性と言います。様々な波長の円二色性の大きさを測定したものを円二色性スペクトルと呼び、タンパク質の円二色性スペクトルの形状は、その立体構造を反映します。したがって、複数のタンパク質の円二色性スペクトルを測定し比較することで、それらの構造に差異があるかどうかを知ることができます。 戻る
- *3 DNA二重鎖切断損傷
- 放射線などによって、二重らせん構造をしているDNAの両方の鎖が切断されてしまう損傷で、がんの発症など重篤な影響を及ぼしかねないDNA損傷の一種。 戻る
- *4 リジン残基
- タンパク質をつくるアミノ酸残基の一種。 戻る
- *5 メチル化
- 分子にCH3が付加されること。付加するCH3の数で、モノ(1個)、ジ(2個)、トリ(3個)メチル化と区別されます。今回調査したリジン残基のメチル化の場合、以下のように変化します。 戻る

- *6 ヒストンタンパク質
- アミノ酸配列の違いなどから、H2A、H2B、H3、H4などに分類されます。DNAはこれらのヒストン各2分子からできた複合体(コアヒストン)に巻き付いて細胞核の中に収納されています。 戻る
- *7 構造
- タンパク質は20種類のアミノ酸がつながってできています。アミノ酸がつながる過程で、アミノ酸の種類やその性質あるいは周りの環境などによって、α-ヘリックスと呼ばれるらせん状の構造やβ-ストランドと呼ばれる直鎖状の構造を取る部分ができます。今回の研究では、これらの構造の割合や構造が形成される位置を調査しました。 戻る
- *8 染色体
- 遺伝子の本体であるDNA分子と多数のヒストンタパク質などで構成される複合体。戻る
- *9 翻訳後修飾
- 細胞内でタンパク質やDNAが合成された後に、特定の分子が付加されること。ヒストンの場合、メチル化の他、アセチル化(CH3COの付加)、リン酸化(H2PO4の付加)などが知られています。最近の研究で、翻訳後修飾により様々な細胞機能の制御が行われていることがわかってきました。 戻る
- *10 エピジェネティック薬
- エピジェネティクスはエピ(epi; 後で付加したという意味)とジェネティクス(genetics; 遺伝学)をつないだ言葉(epigenetics)で、DNA配列によって決まる通常の遺伝現象とは異なり、DNAやヒストンタンパク質の翻訳後修飾により制御される遺伝子機能の変化の仕組み。エピジェネティック(epigenetic; エピジェネティクス的な)薬は、このようなエピジェネティクス変化を利用して薬効を得る薬のこと。 戻る
- *11 VUVCD-NN法
- HiSORで開発された円二色性スペクトルとタンパク質のアミノ酸配列からα-ヘリックス構造とβ-ストランド構造が形成される位置を予測する方法。 戻る
- *12 DNAの転写活性化、抑制化
- DNAに書き込まれた情報を写しとる過程を転写といいます。転写活性化は転写を活発に行うようにすることで、転写抑制化は逆に転写を行わないようにすることを言います。 戻る











